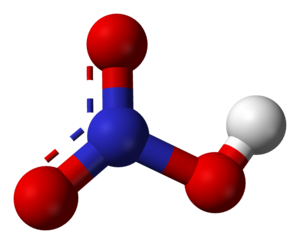
Salpetersuur
|
Algemeen | |
|---|---|
| Naam | Salpetersuur |
 |
 |
| Chemiese formule | HNO3 |
| Molêre massa | 63,01 g/mol |
| CAS-nommer | 7697-37-2 |
| Voorkoms | kleurlose vloeistof tot ligtegeel[1] |
| Reukdrempel | 0,29 dpm |
| Fasegedrag | |
| Smeltpunt | -46,6 °C |
| Kookpunt | 121 °C |
| Digtheid | 1,408 (water=1) |
| Oplosbaarheid | opl. in water |
|
Suur-basis eienskappe | |
| pKa | -1,3 |
|
Veiligheid | |
| Flitspunt | geen |
| LC50 | 244 dpm (rot; 0,5 uur) |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |
Salpetersuur (Engels: Nitric acid of salpetre acid) is 'n baie sterk minerale bytsuur met die molekulêre formule HNO3. Die suiwer verbinding is 'n kleurlose, viskeuse vloeistof, maar ouer monsters is geneig om 'n gelerige skynsel te vertoon as gevolg van die terugval na oksiedes van stikstof en water.
Die meeste kommersieel beskikbare salpetersuur het 'n konsentrasie van 68%. Indien die oplossing meer as 86% HNO3 bevat, word daarna verwys as rokende salpetersuur. Afhangende van die hoeveelheid stikstofdioksied teenwoordig, word die rokende salpetersuur verder geëin as wit rokende salpetersuur, of rooi rokende salpetersuur, teen konsentrasies bo 95%.
Agtergrond
[wysig | wysig bron]Salpetersuur (HNO3) is vroeër vir die vervaardiging van plofstof gebruik, maar dien teenswoordig veral as grondstof vir die kunsmisnywerheid. Die suur is lank reeds bekend en is in die Middeleeue al deur alchemiste gebruik. Salpetersuur (HNO3) is 'n sterk anorganiese suur wat gebruik kan word om chemikalieë met suurstof te laat verbind (te oksideer) of om dit met stikstof te laat verbind (te nitreer).
Dit was reeds in die Middeleeue bekend as aqua fortis (sterk water) en is verkry deur byvoorbeeld salpetererts in water te kook. Die suur is teenswoordig in die handel verkrygbaar as 'n oplossing van 68% HNO3 in water. ʼn Oplossing met 68 % salpetersuur daarin het 'n digtheid van 1 410 kg/ m3 en 'n kook punt van 122 °C, terwyl suiwer salpetersuur ʼn kookpunt van 78 °C en 'n digtheid van 1 520 kg/ m3 het.
Salpetersuur is 'n bytende stof wat byvoorbeeld die vel geel verkleur wanneer dit in 'n verdunde vorm daarmee in aanraking kom. Die suur kan egter ook ernstige brandwonde veroorsaak. Die alchemiste van die Middeleeue het aqua fortis berei deur water saam met salpetererts (KNO3) en kopervitrioel (CuSO4) of ander vitrioele (sulfate) te verhit.
Later is salpetersuur in 'n distillasieproses uit chilisalpeter (NaNO3) en swaelsuur (H2SO4) berei: NaNO3+ H2SO4 → NaHSO+HNO3. Die moderne bereidingsproses berus op die oksidasie van ammoniak in die sogenaamde Ostwald proses. Hierdie proses bestaan uit drie stappe waarby warmte telkens vrygestel word. Die eerste stap verloop by 'n hoë temperatuur (800- 900 °C) in die aanwesigheid van platinum of ʼn platinumrhodiumlegering as katalisator.
Die metaaldrade van die katalisator is in die vorm van gaas geweef wat deur die vrygestelde warmte by 'n bepaalde temperatuur gehou word. Nadat die reaksiemengsel afgekoel het, stel dit stikstofdioksied (NO2) vry wat in gasvorm na ʼn absorpsietoring gelei word om met water of verdunde salpetersuur te reageer. Die dioksied (NO2) los stadig hierin op, terwyl die monoksied (NO) met suurstof geoksideer word.
Die oksidasie veroorsaak die bekende geelbruin rookpluime wat uit stikstofoksiedgasse bestaan. Omdat dit besoedeling veroorsaak (en baie lande wetgewing daarteen het), word die afvalgasse in moderne fabrieke met aardgas-, waterstof- of koolstofmonoksiedhoudende gasse (tot ongeveer 600 °C) verhit, waardeur die stikstofoksied grotendeels gereduseer word.
'n Ander bereidingsproses, waarby heelwat elektrisiteit egter verbruik word, is die vlamboogproses waarby stikstof en suurstof in 'n vlamboogoond regstreeks verhit word om NO2 te vorm. ʼn Belowende ontwikkeling is die verhitting van die 2 elemente in ʼn oond wat van sonenergie gebruik maak.
Die reaksie van stikstof en suurstof (N2+ O2 ↔7 2NO) is 'n newereaksie van alle prosesse waarby lug sterk verhit word; by motorenjins, gasbranders, elektriese vonke, ensovoorts. As gevolg hiervan word groot hoeveelhede stikstofoksied (NO) daagliks in die atmosfeer vrygestel. Die stikstofoksied slaan saam met reën as salpetersuur neer en kan skadelik wees.
Dit kan ook deur sonlig en ultravioletstraling opgebreek word in NO en atomiese suurstof (O), wat baie sterk oksiderend kan werk. In die berugte fotochemiese rookmis word koolwaterstowwe (afkomstig byvoorbeeld uit onverbrande petroldampe) geoksideer tot stowwe soos formaldehied en urasielnitraat, wat baie irriterend vir die slymvliese kan wees. Salpetersuur is sterk oksiderend sowel as nitrerend en word dikwels as beitsmiddel vir metale gebruik.
Yster, chroom en aluminium word nie deur salpetersuur aangetas nie, maar salpetersuur is sterk genoeg om koper, silwer, kwik, fosfor en swael te oksideer. By koolstofverbindings kan daar naas oksidasie ook nitrering plaasvind. Nitrietsuur is 'n mengsel van gekonsentreerde salpeter- en swaelsuur en dit word in die organiese chemie gebruik om verskeie verbindings te nitreer.
Belangrike nitroverbindings is nitrobenseen, trinitrotolueen (TNT, 'n bekende plofstof), trinitrofenol, nitrogliserien (ook ʼn plofstof) en nitrosellulose (wat vir die vervaardiging van plofstof, plastiek en vernis gebruik word). Voorheen was die plofstofnywerheid die grootste verbruiker van salpetersuur, maar teenswoordig gebruik die kunsmisnywerheid ruim 60 % van alle geproduseerde salpetersuur.
In hierdie nywerheid word kunsmisprodukte soos ammoniumnitraat (HN4NO3), kaliumnitraat (KNO3) en kalsiumnitraat (Ca(NO3)2) uit salpetersuur berei. 'n Bekende laboratoriumproduk is koningswater of aqua regia. Dit is ʼn mengsel van gekonsentreerde salpeter- en soutsuur wat edelmetale soos goud en platinum kan oplos.
Die soute van salpetersuur word nitrate genoem en is gewoonlik goed oplosbaar in water. Dit is opmerklik dat die nitrate van byna alle metale geredelik oplosbaar in water is en dikwels in laboratoria gebruik word. Dit ontbind egter vinnig by verhitting en kan selfs ontploffings veroorsaak.
Soute
[wysig | wysig bron]Nitrate is die soute wat afgelei word van salpetersuur.
Anhidraat
[wysig | wysig bron]Die anhidraat van salpetersuur is distikstofpentoksied N2O5.
Laboratoriumvervaardiging
[wysig | wysig bron]Salpetersuur kan in die laboratorium gesintetiseer word deur die verhitting van koper(II)nitraat. Die reaksie lewer die gasse stikstofdioksied en suurstof op, wat dan deur water herlei word om salpetersuur te gee.
- 2 Cu(NO3)2 → 2 CuO(s) + 4 NO2(g) + O2(g)
Fisiese eienskappe
[wysig | wysig bron]| Massa % HNO3 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Digtheid (g/cm3) |
1,00 | 1,05 | 1,12 | 1,18 | 1,25 | 1,31 | 1,37 | 1,42 | 1,46 | 1,48 | 1,513 |
| Viskositeit (mPa·s) |
1,00 | 1,04 | 1,14 | 1,32 | 1,55 | 1,82 | 2,02 | 2,02 | 1,84 | 1,47 | 0,88 |
| Smeltpunt (°C) | 0 | −7 | −17 | −36 | −30 | −20 | −22 | −41 | −39 | −60 | −42 |
| kookpunt (°C) | 100,0 | 101,2 | 103,4 | 107,0 | 112,0 | 116,4 | 120,4 | 121,6 | 116,6 | 102,0 | 86,0 |
| Parsiële druk (HNO3) (mbar) | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,3 | 1,2 | 3,9 | 14,0 | 36,0 | 60,0 |
| Parsiële druk (H2O) (mbar) | 23,3 | 22,6 | 20,2 | 17,6 | 14,4 | 10,5 | 6,5 | 3,5 | 1,2 | 0,3 | 0,0 |
| HNO3 (mol/l) | 1,7 | 3,6 | 5,6 | 7,9 | 10,4 | 13,0 | 15,8 | 18,5 | 21 | 24,01 |
Gebruike
[wysig | wysig bron]Die hoofgebruik vir salpetersuur is in die vervaardiging van kunsmis. Die salpetersuur word met ammoniak geneutraliseer om ammoniumnitraat te vorm. Hierdie aanwending verbruik 75–80% van die 26 miljoen ton wat jaarliks geproduseer word (1987).
Ander aanwendings is in die vervaardiging van plofstowwe, nylonvoorlopers en ander spesialis-organiese verbindings.[2]
Kyk ook
[wysig | wysig bron]Verwysings
[wysig | wysig bron]- ↑ SciLab Msds.
- ↑ 2,0 2,1 Michael Thiemann, Erich Scheibler, Karl Wilhelm Wiegand, "Nitric Acid, Nitrous Acid, and Nitrogen Oxides" in Ullmann Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim.
Bronne
[wysig | wysig bron]- Wêreldspektrum, 1982, ISBN 0908409656, volume 24, bl. 209
Notas
[wysig | wysig bron]| Hierdie artikel is in sy geheel of gedeeltelik vanuit die Engelse Wikipedia vertaal. |