Tripolifosfato de sódio
| Tripolifosfato de sódio Alerta sobre risco à saúde | |
|---|---|
| |
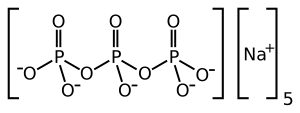
| Nome IUPAC | sodium triphosphate |
| Identificadores | |
| Número CAS | |
| PubChem | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | Na5O10P3 |
| Massa molar | 367.86 g/mol |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O tripolifosfato de sódio (TPF) ou tripolifosfato pentassódico ou ainda trifosfato de sódio é um composto de fórmula química Na5P3O10, número CAS: 7758-29-4, que se apresenta comercialmente na forma de pó branco de densidade aparente 0,7 a 1 g/cm3. Apresenta ponto de fusão variando de 650 a 1000 °C. Sua solução aquosa a 1%, a 25 °C, apresenta pH 9,5 a 10,5. Possui peso molecular de 367,88 g/mol. É inodoro.
Usos
[editar | editar código-fonte]É utilizado como agente de flotação, dispersante, emulsificante, estabilizante de solos, sequestrante e como reforçador em produtos destinados a limpeza, como detergentes e sabões em pó.[1]
Encontra aplicações em ramos de atividade e indústrias tão variados quanto na agricultura, alimentícia, argila e pigmentos, borracha, cimento e cerâmica, construção civil, domissanitários, detergentes e produtos de limpeza, lubrificantes, papel e celulose, pastas para os mais diversos fins, industrias petrolíferas, têxtil e formuladores têxteis, tintas e vernizes, tratamento de água, vidraria, tratamento de superfície e formuladores.
Esta substância também é utilizada como estabilizante para os leites "longa vida" ou "UHT"...
Obtenção
[editar | editar código-fonte]Industrialmente o tripolifosfato de sódio é preparado por aquecer uma mistura estequiométrica de fosfato dissódico, Na2HPO4 e fosfato monossódico, NaH2PO4 em condições cuidadosamente controladas.[2]
- 2 Na2HPO4 + NaH2PO4 → Na5P3O10 + 2 H2O
- [3]
Efeitos ambientais
[editar | editar código-fonte]O seu uso como reforçador em detergentes tanto domésticos quanto industriais em grande quantidade e posterior eliminação nos sistemas de esgotos sem adequado tratamento causa o incremento da concentração de fósforo nas águas de diversos mananciais.
Este aumento de sua concentração nestas massas de água causa o aumento do crescimento de organismos dependentes do fósforo, como são as algas. Estes organismos usam grandes quantidades de oxigênio e evitam que os raios de sol entrem no água. Isto torna tais águas pouco adequadas para a sobrevivência de outros organismos. O fenômeno é denominado de eutrofização.
- ↑ Viktoria Klara Lakatos Osorio e Wanda de Oliveira; POLIFOSFATOS EM DETERGENTES EM PÓ COMERCIAIS; Quím. Nova vol.24 no.5 São Paulo Sept./Oct. 2001 - www.scielo.br
- ↑ Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements, 2nd Edition, Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ↑ «Sodium tripolyphosphate 7758-29-4 wiki». GuideChem (em inglês). Consultado em 20 de setembro de 2023