“生きた神経細胞”を脳にインプラント。脳と機械の接続に一歩前進?【研究紹介】
2024年12月6日
先端テクノロジーの研究を論文ベースで記事にするWebメディア「Seamless/シームレス」を運営。最新の研究情報をX(@shiropen2)にて更新中。
米国の医療技術チーム「Science Corporation」に所属する研究者らが発表した論文「Optogenetic stimulation of a cortical biohybrid implant guides goal directed behavior」は、脳とコンピュータをつなぐインターフェース(BCI。BMIとも)の新しいアプローチとして、生きた神経細胞とデバイスを組み合わせたバイオハイブリッド型の装置を開発した研究報告である。
研究内容
従来のBCIでは、電極を脳組織に直接刺入する必要があり、これによって引き起こされる組織損傷、炎症反応、瘢痕形成が大きな問題となっていた。これらの反応により、電極周辺の神経細胞が失われ、長期的な神経活動の記録が困難になることが知られている。
今回開発された生体ハイブリッドインプラントは、脳の皮質表面に設置するだけで、その中に含まれる神経細胞が脳の細胞と接続を形成でき、組織破壊がより少ない可能性がある。
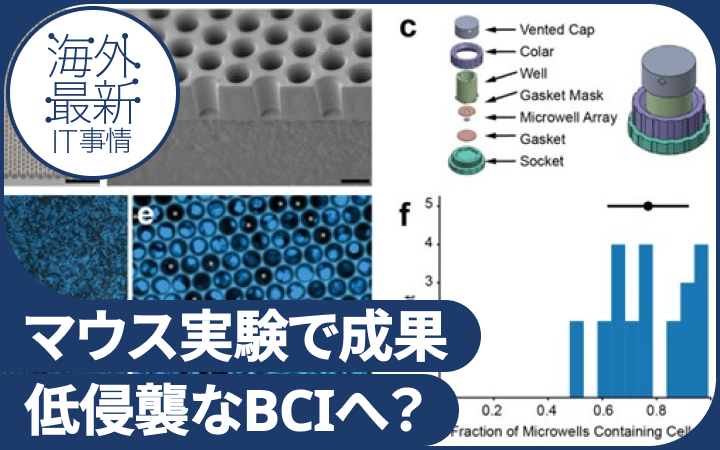
具体的には、直径10マイクロメートルの円形の微小なマイクロウェルを高密度に配置した足場構造を開発した。この構造は、光を通す材料で作られており、1つのマイクロウェルに1個の神経細胞を収容できるよう設計されている。25平方ミリメートルの面積に約11.8万個のマイクロウェルが配置されており、高密度な神経細胞のインターフェースが可能となっている。
このインプラント装置の神経細胞は細胞突起を伸ばすことができ、それによって脳へ信号を伝達することが可能と考えられる。
移植する神経細胞は、マウスの胎児から採取した大脳皮質神経細胞を用いた。これらの細胞は、光刺激に応答するタンパク質を発現するように遺伝子改変され、マイクロウェルに導入された。実験では、平均して77%のマイクロウェルに細胞を導入することに成功した。つまり、このインプラント装置には、平均約9万個の生きた神経細胞が組み込まれている。
装置を大脳皮質表面に移植すると、光刺激に応答するタンパク質を発現した細胞の約52%が3週間後も生存していることが確認された。これは、従来の神経細胞移植での生存率(25%未満)を大きく上回る結果である。移植された細胞は自発的な活動を示し、脳の表層に突起を伸ばして宿主の脳と結合することも観察された。
マウス実験
研究チームは、この装置の機能を実証するべく、マウスに訓練を施し、光刺激の有無を判断するための行動実験を行わせた。実験装置には、3つのポート(小さな穴)がある。マウスが中央のポートで試行を開始し、生体ハイブリッドインプラントに光刺激があった場合は左のポート、なかった場合は右のポートを選択すると水の報酬が得られる仕組みとした。
実験の結果、9匹中5匹のマウスが3週間の訓練期間内に課題を習得し、光刺激を正確に検知できるようになった。マウスは光を直接見ることができないにもかかわらず、反応を示したことから、インプラント装置の光感受性ニューロンがマウスの脳と接続を形成したことが示唆されている。
この成功率は、直接脳に遺伝子導入して光感受性を持たせた対照群(7匹中6匹が成功)と統計的な優位差がないレベルであった。また、課題を習得したマウスは、1秒あたり最高で0.7ビットの情報伝達率を達成した(平均値は0.25ビット/秒)。
Source and Image Credits: Jennifer Brown, Kara M. Zappitelli, Paul M. Dawson, Eugene Yoon, Seton A. Schiraga, Amy E. Rochford, Mohamed Eltaeb, Arturo Rodriguez, Yifan Kong, Max Hodak, Alan R. Mardinly. Optogenetic stimulation of a cortical biohybrid implant guides goal directed behavior. bioRxiv 2024.11.22.624907; doi: https://doi.org/10.1101/2024.11.22.624907
関連記事
ミニ脳16個入「バイオプロセッサ」 消費電力通常の100万分の1、APIでアクセス可能、研究者向けサブスクも【研究紹介】
人間の脳組織を3Dプリンタで印刷。成長し神経ネットワークを形成、疾患研究への応用に期待 米研究者ら発表【研究紹介】
猫に“ニット帽”で脳波記録。計測器やさしく固定、できるだけストレス与えず【研究紹介】
人気記事